MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN DE SUSTANCIAS ORGÁNICAS
INTRODUCCIÓN
Cuando se quiere conocer la composición de una sustancia
orgánica es necesario seguir tres etapas básicas.
Obtener una muestra representativa de la muestra.
Separar o aislar cada una de las sustancias componentes de la
mezcla para su posterior análisis.
La segunda de las etapas es una de las más complejas,
laboriosas y difícil de realizar
El conocimiento de los métodos de aislamiento y purificación
de un compuesto es fundamental en Química Orgánica por las
siguientes razones:
• Poder determinar su estructura
• En los procesos de síntesis.
• Seguimiento de las reacciones químicas
Estos métodos están basados en las diferencias que existen
entre las propiedades físicas de los componentes de una mezcla
(puntos de ebullición, densidad, presión de vapor,
solubilidad, etc.)
Los métodos de separación explicados en esta entrada serán los siguientes:
Filtración, Decantación, Cristalización, Sublimación, Destilación, Extracción y Cromatografía
FILTRACIÓN
Se conoce como filtración a una técnica para separar sólidos en suspensión dentro de un fluido (líquido o gas), empleando para ello un medio filtrante: un sólido poroso que pasa a denominarse tamiz, filtro o criba. Este filtro retiene los sólidos de mayor tamaño y permite el paso del fluido, junto con las partículas de tamaño inferior.
Consiste en retener partículas sólidas suspendidas de un
líquido o un gas forzando la mezcla a través de una barrera
porosa que puede ser mallas, fibras, material poroso o un
relleno sólido.
FILTRACIÓN POR SUCCIÓN
La filtración a vacío o por succión se utiliza para mezclas
como barros y pastas.
El agua al pasar a través de la trompa, en el estrechamiento
interior, aumenta su velocidad originando una disminución de
presión. Esto origina una succión del aire a través de la
conexión con el matraz, originando un pequeño vacío en éste.
También se emplea para separar los cristales obtenidos a
partir de una disolución.
DECANTACIÓN
 La decantación es una técnica que permite separar un sólido mezclado heterogéneamente con un líquido en el que es insoluble o bien dos líquidos inmiscibles (que no se pueden mezclar homogeneamente) con densidades diferente.
La decantación es una técnica que permite separar un sólido mezclado heterogéneamente con un líquido en el que es insoluble o bien dos líquidos inmiscibles (que no se pueden mezclar homogeneamente) con densidades diferente.
CRISTALIZACIÓN
Proceso de separación de un soluto a partir de su disolución,
por sobresaturación de la misma, aumento de la concentración o
por enfriamiento de esa disolución.
La cristalización permite separar solutos prácticamente puros.
CRISTALIZACIÓN POR EVAPORACIÓN
Esta es la otra opción para lograr la
precipitación de los cristales de soluto, haciendo uso de un proceso de
evaporación de solvente (a temperatura constante, a diferencia del método
anterior), para hacer así que la concentración de soluto sobrepase el nivel de
solubilidad.
SUBLIMACIÓN
Es el paso de una sustancia del estado sólido al gaseoso sin
pasar por el estado líquido. Se puede considerar como una
forma especial de destilar una sustancia sólida.
La temperatura de sublimación es aquella a la cual la presión
de vapor del sólido iguala a la presión externa.
Para que una sustancia sublime debe tener una elevada presión
de vapor, es decir, las atracciones intermoleculares en estado
sólido deben ser débiles
Cuanto menor sea la diferencia entre la presión externa y la
presión de vapor de una sustancia más fácilmente sublimará.
La sublimación es un método excelente para la purificación de
sustancias relativamente volátiles.
Ejemplos: la desaparición de la nieve, sin fundir, en un día
de invierno frío pero soleado, el dióxido de carbono sólido,
la naftalina y el yodo que subliman a la temperatura
ambiente.
DESTILACIÓN
La separación y purificación de líquidos por destilación
constituye una de las principales técnicas para purificar
líquidos volátiles. La destilación hace uso de la diferencia
entre los puntos de ebullición de las sustancias que
constituyen una mezcla.
 Las dos fases en una destilación son la vaporización o
transformación del líquido en vapor y la condensación o
transformación del vapor en líquido. Existen varios tipos de
destilaciones. La elección en cada caso se hace de acuerdo con
las propiedades del líquido que se pretenda purificar y de las
impurezas que lo contaminan.
Las dos fases en una destilación son la vaporización o
transformación del líquido en vapor y la condensación o
transformación del vapor en líquido. Existen varios tipos de
destilaciones. La elección en cada caso se hace de acuerdo con
las propiedades del líquido que se pretenda purificar y de las
impurezas que lo contaminan.
El método físico consiste en suministrar calor a la mezcla
logrando que el líquido de menor punto de ebullición se
vaporice en primer lugar y luego se produzca la condensación
de ese vapor al ponerlo en contacto con una superficie fría.
DESTILACIÓN SIMPLE
Técnica utilizada en la purificación de líquidos cuyo punto de
ebullición es inferior a 150ºC a la presión atmosférica.
Útil para eliminar impurezas no volátiles
También sirve para separar dos líquidos con puntos de
ebullición que difieran en al menos 25 ºC.
DESTILACIÓN A VACÍO O PRESIÓN REDUCIDA
Técnica usada en la separación de líquidos con un punto de
ebullición superior a 150 ºC.
Como un líquido hierve cuando su presión de vapor iguala la
presión atmosférica, se puede reducir su punto de ebullición
disminuyendo la presión a la cual se destila
Para mantener una ebullición homogénea se puede usar plato
poroso o adaptar al conjunto un capilar para mantener la
ebullición homogénea.
DESTILACIÓN FRACCIONADA
Técnica que se utiliza en la separación de sustancias cuyos
puntos de ebullición difieren entre sí menos de 25ºC.
La diferencia con la destilación simple es que incorpora una
columna de fraccionamiento (o de rectificación) entre la
disolución y el refrigerante.
La columna de fraccionamiento consta de un tubo largo de
vidrio que lleva en su interior un relleno inerte (hélices de
vidrio) o unos platos de condensación.
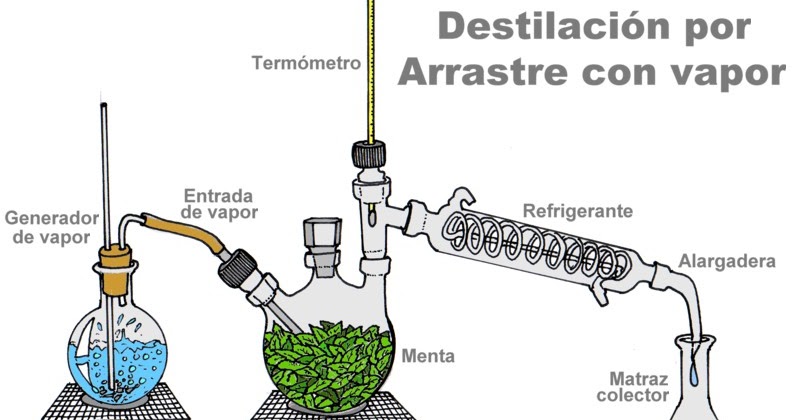
DESTILACIÓN EN CORRIENTE DE VAPOR
Al hacer pasar una corriente de vapor a través de la mezcla,
ambos componentes se destilan juntos.
Como el agua y el compuesto son inmiscibles, cada uno de
ellos ejerce su presión de vapor independientemente del otro
(al contrario que en la destilación simple)
EXTRACCIÓN
Se aplica a todo tipo de mezclas ya sean sólidas, líquidas o
gaseosas.
Está fundamentada en la diferencia de solubilidades de los
compuestos.
CROMATOGRAFÍA
Se entiende por cromatografía al conjunto de técnicas
analíticas que se fundamentan en la separación que se produce
cuando una mezcla de compuestos es arrastrada por una fase
móvil a lo largo de una fase estacionaria.
La técnica cromatográfica de purificación consiste en separar
mezclas de compuestos en función de su diferente afinidad
entre una fase estacionaria y una móvil.
CLASIFICACIÓN DE LOS PROCESOS CROMATOGRÁFICOS
La fase móvil puede ser un líquido o un gas. La fase
estacionaria puede ser un sólido o un líquido.
Teniendo en cuenta la naturaleza de la fase estacionaria se
establece la siguiente clasificación.
 CROMATOGRAFÍA DE ADSORCIÓN: la fase estacionaria es un sólido
sobre el que se adsorben los componentes de la muestra.
CROMATOGRAFÍA DE ADSORCIÓN: la fase estacionaria es un sólido
sobre el que se adsorben los componentes de la muestra.
- Cromatografía Líquido – Sólido CLS (fase móvil líquido)
- Cromatografía Gas – Sólido CGS (fase móvil gas)
- Cromatografía en Capa Fina CCF
(fase estacionaria sólida en forma plana y la móvil
líquida)
CROMATOGRAFÍA DE REPARTO: la fase estacionaria es un líquido
sostenido por un sólido inerte.
- Cromatografía Líquido – Líquido CLL (fase móvil un
líquido)
Fase Móvil
Fase Estacionaria
Soluto - Cromatografía Gas – Líquido CGL (fase móvil un gas)
- Cromatografía en papel (fase estacionaria es una capa de
agua adsorbida sobre una hoja de papel)
CROMATOGRAFÍA DE INTERCAMBIO IÓNICO: la fase estacionaria es
una resina de intercambio iónico y la separación se produce
por la unión de los iones a la fase estacionaria.
CROMATOGRAFÍA DE EXCLUSIÓN MOLECULAR: la fase estacionaria es
una estructura parecida a un tamiz y la separación se produce
en función del tamaño de las moléculas.
Teniendo en cuenta la forma de la fase estacionaria se
clasifica en:
- Cromatografía en columna
- Cromatografía plana (cromatografía en capa fina y en
papel.
Por: Equipo 7 - 2AVQ


RIOS MAR DIANA GABRIELA:
ResponderBorrarLos métodos de separación y purificación de sustancias están basados en las diferencias que existen entre las propiedades físicas que existen entre los componentes de la muestra como lo es el punto de ebullición, densidad, presión de vapor, solubilidad, etc y es de mucha importancia conocer este tipo de procedimientos cuando se requiere separar una muestra, y es lo que esté tema nos explica por lo tanto me parece muy buena la información que aquí se presenta
La separación y la purificación se sustancias y compuestos nos sirve ya sea para separar sustancias de otras, para ver los componentes que la conforman o tener un compuesto puro.
ResponderBorrarEsta información es muy buena ya que nos ayuda a saber como se realiza cada método de separación en el laboratorio así como sus riesgos que hay que tener en cuenta para no tener ningún accidente al momento de realizar cada uno de estos métodos por lo que se me hace una información muy completa y bien descrita con cada paso a seguir. Nicole Michelle Castro Fernández.
ResponderBorrarLos metodos de separación y purificación son esenciales para el uso de la vida ya que podemos extraer o deshacernos de dichos componenetes que traen una sustancia
ResponderBorrarEste tema se me hace sumamente importante ya que es así como podemos separar compuestos o sustancias, hay algunos que usamos más que otros ya que son más conocidos, comunes o simplemente es el método que necesitamos en ese momento, en general me pareció muy buena la información y bien redactado
ResponderBorrarSánchez Luna Silvia Areli
Los métodos de separación y purificación son utilizados en el laboratorio para separar dos sustancias o reactivos. Estos son esenciales en los procesos utilizados el industria química.
ResponderBorrarLos métodos de separación y purificación de sustancias, son muy útiles para cuando se necesitan separar o purificar dos o más sustancias o compuestos. Estos métodos fueron creados a consecuencia de las diferentes características físicas que cada sustancia puede tener, así que, para cada diferente característica, existe un diferente método de separación para realizarlo correctamente, siguiendo los pasos adecuados.
ResponderBorrarCASTILLO DON JUAN JOHANA GUADALUPE.
ResponderBorrarLa información presentada es clara y concreta además de que muestra de forma definida el concepto de cada método de separación y purificación, los cuales nos han sido de mucha ayuda durante el semestre para la purificación de compuestos y separación de varias sustancias además de que con estos métodos de pueden llegar a realizar productos caseros como en el caso de la destilación por arrastre de vapor extrayendo una esencia etc.
CASTILLO DON JUAN DIANA GUADALUPE
ResponderBorrarEs importante mencionar y tener los conocimientos necesarios para llevar a cabo un método de purificación de mezclas dado que cada una cuenta con propiedades fisicoquímicas diferentes y es por ello que se debe de escoger el método adecuado para poder separar el compuesto de interés considerando la densidad, solubilidad, puntos de ebullición etc.
Es importante saber cuáles son los tipos de separación ya que los utilizamos en el laboratorio al momento de separar las mezclas.
ResponderBorrar~ Cervantes Adán María Guadalupe.
ResponderBorrarComo sabemos, las técnicas de separación y purificación son métodos utilizados, mayormente en química orgánica, en base a las propiedades físicas de los componentes que conforman a una mezcla.
Hay técnicas que se realizan a partir de la diferencia de temperatura de los componentes de una solución, tal es la destilación,entre otros factores que influyen en estos procesos. Es una información que nos brinda conceptos g ejemplos, lo cual la hace información clara.
Los Métodos de Separación se basan en diferencias entre las propiedades físicas de los componentes de una mezcla, tales como: Punto de Ebullición Densidad, Presión de Vapor, Punto de Fusión, Solubilidad, etc.
ResponderBorrarMARÍA DEL CARMEN ROBERTO RAMOS